Согласование постаналитического этапа согласно стандарту ISO 15189:2023

Постаналитический этап тестирования признан фундаментальным для повышения качества и эффективности лабораторной информации. Данные показывают, что этот этап является окном возможностей для инициатив усовершенствования и гармонизации, но ему уделяют недостаточно внимания. В статье будет рассмотрен лабораторный отчет согласно стандарту ISO 15189:2023.
Стандарт ISO 15189:2023
Стандарт ISO 15189:2023 для аккредитации медицинских лабораторий определяет постаналитическую фазу как «процессы, происходящие после обследования, включая просмотр результатов, форматирование, обнародование, отчетность и сохранение результатов обследования, содержание и хранение клинического материала, образца и утилизация отходов». Это определение, однако, не учитывает этапы, которые выполняются после передачи лабораторных отчетов и которые являются решающими для замыкания цикла:
- подтверждение получения данных;
- интерпретация;
- использование;
- дальнейшее наблюдение;
- документирование.
Эти шаги были сгруппированы в так называемую «пост-пост-аналитическую фазу». Даже если эти последние шаги цикла не находятся под прямым контролем лабораторных специалистов, они являются важными переменными, которые влияют как на ценность лабораторной информации, так и на результат пациента.
От данных к информации
Данные - это числа, величины, сущности и факты, такие как, например, результаты лабораторных исследований. Однако информация генерируется, когда этим данным придается значение, поскольку данные без интерпретации являются фактами без понимания. В случае лабораторных результатов, числовые данные должны сопровождаться другими параметрами, которые обычно определяются как «компараторы» (главным образом, но не только, терминологией, единицами измерения, контрольными значениями, пределами принятия решения и интерпретационными комментариями), направленными на то, чтобы сделать данные «пригодными». С точки зрения пользователя, будь то врач или пациент, преобразование данных в полезную информацию является единственным, что имеет значение, поскольку именно эта информация, а не необработанные аналитические результаты, влияет на клинические рассуждения и принятие решений. В то время как специалисты лаборатории, прежде всего, должны обеспечивать точность и надежность лабораторных результатов, сообщение об аналитических результатах должно сопровождаться другими важными инструментами, которые позволяют правильно интерпретировать и использовать лабораторную информацию для процесса принятия клинических решений и лечения пациентов. Необходимость усовершенствования постаналитической фазы была синтезирована как «хорошее постаналитическое качество делает хорошую лабораторную информацию», признавая пять прав, которые должны быть достигнуты, чтобы гарантировать, что аналитические результаты имеют значение и ценность. Только таким образом лабораторная информация может соответствовать конечной цели лабораторной медицины, которая заключается в улучшении результатов здоровья.
Гармонизация постаналитической фазы: отчет
Поскольку это в основном требует общения с участием сторон (то есть лаборантов, врачей, специалистов по информационным технологиям и пациентов), которые говорят на разных языках, постаналитическая фаза гармонизации является достаточно сложной проблемой. В частности, лабораторный отчет является залогом предоставления пользователям правильной информации. В своей основополагающей статье 1976 года, опубликованной в Lancet под названием «Отчеты о клинической химии. Проблемы и предложения", Алан М. Болд отметил необходимость „стандартизации форматов отчетов“, предложив отчитываться о 13 пунктах, 7 из которых были определены как „существенные“, а остальные 6 как „дополнительные функции“, как указано в таблице ниже „Лабораторный отчет: общие требования“.
Лабораторный отчет: общие требования
| Существенные | Дополнительные функции |
|
|
Болд также подчеркнул, что «все отчеты должны включать указания относительно патологий, быть в кумулятивном формате и содержать реалистичное утверждение об аналитической надежности». К сожалению, спустя несколько десятилетий имеющиеся доказательства демонстрируют низкое соответствие описанным требованиям, что, кроме того, мало уделялось внимания в литературе. Требования к постаналитической фазе, которая называется процессами после экспертизы, описаны в подпунктах 7.4.1 и 7.4.2 международного стандарта ISO 15189 как «отчет о результатах», «пересмотр результатов и выпуск», «критические отчеты о результатах», «особое внимание к результатам», «дополнительная информация для отчетов», «поправки к отчетным результатам» и «обработка образцов после исследования». В документе некоторых рабочих групп Европейской федерации лабораторной медицины (EFLM) подчеркивается необходимость использования ISO 15189 как «систематической основы для совершенствования практики обнародования результатов, чтобы предложить критерии для процедур для получения соответствующего отчета о результатах.
Управление обнародованием результатов должно быть направлено на предотвращение ошибочных выводов без задержки распространения данных, которые являются важными и точными. Улучшенное представление лабораторной информации может способствовать быстрой интерпретации и более точному диагнозу и лечению. Однако представленный отчет показывает, что большинство лабораторий не в состоянии отразить надлежащие усилия в предоставлении высококачественных аналитических данных в кратчайшие сроки с минимальным уровнем ошибок в течение всего медицинского обслуживания. Они не используют полноценно современные решения информационных технологий или автоматизированную обработку для агрегации данных.
Основные требования к лабораторному отчету
Лабораторный отчет должен содержать по крайней мере данные о:
- личности пациента;
- время получения образца;
- единицы измерения;
- референтные интервалы и/или границы клинического решения, если они доступны;
- терапевтический диапазон для препаратов и пояснительные комментарии, если это необходимо.
Требования к отчетам, описанные в ISO 15189, в пунктах 7.4 «Процессы после обследования» и 7.2 «Процессы перед обследованием», включают важные требования о необходимости «однозначного отслеживания пациента к запросу и образца, идентификации и контактная информация запрашивающего, идентификация запрашиваемой (их) экспертизы». Важно, что международный стандарт рекомендует, чтобы «результаты обследования сообщались точно, четко, недвусмысленно и в соответствии с любыми конкретными инструкциями в процедуре обследования», таким образом подчеркивая взаимосвязи между различными этапами процесса тестирования.
В стандарте подчеркивается важность термина «однозначная идентификация», поскольку в нем указано, что «Идентификаторы логического наблюдения имен и кодов (LOINC) и номенклатура свойств и единиц (NPU, NGC) и SNOMED CT являются примерами электронной идентификации. Терминология в отчете должна совпадать с согласованными на международном уровне системами (например, системами идентификаторов логических наблюдений и кодов (LOINC) или системами номенклатуры свойств и единиц (NPU)), а использование международной системы единиц (SI) должно способствовать».
Обмен результатами лабораторных исследований между различными поставщиками медицинских услуг требует стандартизированной терминологии, используемой для четкого определения:
- лабораторного теста (например, «культура бактерий»);
- исследуемые свойства (тип свойства, такой как «концентрация альбумина в плазме крови»);
- типы образцов (например, артериальная кровь, 24-часовой сбор мочи, спинномозговая жидкость);
- анатомическое расположение образца (например, образец из кожи левого колена);
- аналиты (компоненты или элементы, такие как натрий, аланинтрансаминаза, антитела к бруцелле);
- тип измеряемого свойства (например, концентрация массы, объем, количество фракций);
- результаты для номинальных или порядковых значений результата (скорость, частота, масса и т.д.);
- единицы, в которых представлено значение (для количественных значений результата).
Документ также рекомендует, чтобы «поскольку страны-члены используют различные лабораторные системы кодирования, следует учитывать не только код и название теста, но и дополнительные составляющие спецификации теста и результата».
Таким образом, четко необходима гармонизация на постаналитической фазе для трансграничной помощи, что имеет решающее значение для обеспечения согласованности и избежания фрагментации и дублирования запросов на тестирование, но такая же согласованность должна быть гарантирована на местном, региональном, национальном и международном уровнях. Однако, по словам Роберта Флетмана, «текущие вариации на практике по номенклатуре, референтных интервалов, маркировки, единиц, стандартизации и прослеживаемости между аналитическими методами, а также представление кумулятивных данных результатов являются неэффективными и неудобными, или, что еще хуже, угрожают безопасности пациентов. Все аспекты лабораторных услуг во всем процессе тестирования в конечном итоге зависят от сжатого, надежного общения». Существует высокий риск ошибок в текущих форматах отчетов, включая «неправильное толкование с различными единицами, по сравнению с референтными интервалами и хронобиологией, непонимание различий методов в результатах и вариации в обозначении неправильных результатов». Хотя понятно, что аналитический результат всегда должен предоставляться с единицей, передача результата без единицы основывается на предположении, что получатель знает правильную единицу. Хотя это редко может быть проблемой на местном уровне для обычных анализов, многие анализы на лекарства и гормоны часто оцениваются в разных подразделениях между лабораториями, штатами и странами. Если единица предоставляется, клиницист все равно может непреднамеренно предположить использование единицы от другого поставщика тестов, с которым он знаком.
Величина результата часто сильно отличается для одного и того же аналита, приведенного в разных единицах, и эти различия иногда могут быть опасно незначительными или представлять риск для безопасности пациента. Это было описано, например, для результатов гемоглобина, которые иногда выражаются не в г/л (правильные единицы), а в г/дл (10- кратная разница).
Даже если во время «бумажной эры» появились вариации в лабораторных отчетах, некоторые факторы сейчас ставят под угрозу надежность новых электронных систем, которые должны обеспечивать функциональную совместимость (связь и получение фактического сообщения между аппаратным обеспечением, программным обеспечением и людьми) и семантическую совместимость (успешное кодирование и декодирование передаваемой информации).
Кроме того, электронные отчеты должны обеспечивать:
- гибкость для отображения результатов, доступных и понятных для медицинского персонала и пациентов;
- функциональность для отображения дополнительной информации;
- параметры фильтрации сложности;
- доступ к лабораторным данным о производительности;
- функциональность для уточнения места группировки или разделения результатов является уместным;
- графическое представление совокупных результатов.
Неопределенность измерения
Погрешность измерения (Measurement uncertainty - MU) является неотъемлемым свойством любого количественного результата измерения, которое выражает отсутствие знания истинного значения результата и включает факторы, которые, как известно, влияют на него. Результат измерения является лишь приближением или оценкой значения измеряемой величины и, таким образом, завершается только тогда, когда сопровождается утверждением о неопределенности этой оценки. Поскольку изменчивости лабораторных результатов не избежать, результат любого измерения представляет собой приближение или оценку значения измеряемой величины и, таким образом, является полным только тогда, когда сопровождается утверждением о неопределенности этой оценки. Погрешность измерения - это не только количественная оценка сомнений относительно результата измерения и ценный показатель качества результата, но и существенная информация, без которой результаты измерений нельзя осмысленно интерпретировать.
Обоснованием для включения MU в лабораторные отчеты является то, что диагностическая неопределенность может вытекать из неполной информации в лабораторных отчетах, что приводит к повышенному риску несоответствующей интерпретации лабораторных данных. Согласно ISO 15189 (подпункт 7.3.4) «Информация MU должна быть доступна пользователям лаборатории по запросу» и, следовательно, даже если MU не включено в атрибуты отчета и не может считаться определенным постаналитическим требованием, рекомендуется как информация, которая должна способствовать надлежащей интерпретации количественных результатов (количественных значений). Фактически, для многих лабораторных тестов аналитическое качество (на основе установленных спецификаций производительности) может меняться со временем и должно быть улучшено благодаря лучшим диагностическим системам и/или высшему соответствию спецификациям аналитических характеристик (APS). Таким образом, правильная интерпретация возможна только на основе знания неопределенности лабораторных результатов, которая является результатом как аналитических (например, предубеждение и неточность), так и других возможных источников неопределенности (например, преданалитические проблемы).
Наведений підпункт ISO 15189 виглядає неоднозначним, оскільки включення MU «за запитом» є, перш за все, дуже складним з практичної точки зору, і, по-друге, це не дозволяє багатьом користувачам отримувати інформацію, яка може покращити інтерпретацію даних лабораторних досліджень. За останнє десятиліття, співробітники відділу лабораторної медицини лікарні університету Падуї, включили до лабораторних звітів інформацію про помилку загальної аналітичної помилки (TAE) і RCV (стандартне значення зміни) для вимірюваних величин, які частіше використовуються для моніторингу пацієнтів, після залучення клініцистів в обговоренні корисності цієї інформації. Нещодавно в документі, присвяченому звіту про MU у звіті лабораторії, ми запропонували замінити TAE на MU, щоб відповідати поточному найсучаснішому рівню, як показано на рисунку.
Сообщение о MU в отчетах лаборатории
Референтные интервалы (RI) и границы принятия решений
Референтные интервалы (RI) и пределы решения (DL) являются ценным инструментом для интерпретации результатов и являются важной частью лабораторного отчета и наиболее часто используемым инструментом сравнения в лабораторной медицине. RI, статистические доверительные пределы для типичного распространения результатов, которые можно найти в здоровой референтной популяции, предназначены для подтверждения здоровья (отсутствия каких-либо заболеваний) с высокой специфичностью (обычно 95%). Существуют некоторые специальные формы референтных лимитов для веществ, которые обычно не встречаются у здоровых людей, например, терапевтические диапазоны уровней лекарств, лимиты обнаружения токсинов (или наркотических веществ), разрешенные лимиты, например, для алкоголя.
Установление RI с использованием «прямых методов» предусматривает определение и отбор референтной популяции, сбор образцов, аналитические измерения и статистический анализ. Были описаны статистические методы для нескольких аспектов установления RI, включая соответствующее выявление и удаление выбросов, распределение RI по переменным (например, по возрасту и полу) и вычисление доверительных интервалов (CI) вокруг контрольных границ. В идеале на RI должно влиять только обслуживаемое население, а не используемые аналитические системы, при условии, что они достаточно гармонизированы или стандартизированы. В эпоху больших данных так называемый «косвенный подход», основанный на использовании больших объемов данных, которые уже хранятся в лабораторных базах, для определения и/или верификации RI, пропагандировал заменить прямой подход. Косвенный подход предлагает несколько преимуществ перед обычным прямым подходом, включая снижение затрат и более простое применение в конкретных возрастных группах, и много косвенных алгоритмов было разработано для определения RI.
Для многих измеряемых величин использование больших данных может обеспечить дополнительный подход к традиционному методу определения общего RI, которому часто мешают теоретические и практические проблемы. Однако настоящий вопрос заключается в выборе между RI и DL. Границы принятия решений являются более клинически ориентированными, поскольку они связаны с конкретным клиническим состоянием и, как правило, имеют целью подтвердить наличие конкретного заболевания или клинического риска с соответственно высокой чувствительностью.
Были определены некоторые показатели для экстрааналитического этапа лабораторных исследований и, в частности, относительно полезности отчетности о RI и DL, а именно:
- правильное использование RI по сравнению с DL;
- обычный по сравнению со специфическим для лаборатории RI;
- правильное использование референтного интервала, связанного с полом;
- правильное использование референтного интервала, связанного с возрастом.
Преимущества DL, в частности в соблюдении рекомендаций по клинической практике и определении аналитических целей, были доказаны в случае, общего холестерина и холестерина ЛПНП при дислипидемии, глюкозы и HbA1C при диабете и сердечного тропонина при острой коронарной болезни.
Изменение референтного значения
Для мониторинга серийных результатов совокупность доказательств указывает на то, что так называемое изменение референтного значения (RCV) следует рекомендовать как более эффективный компаратор, чем RI и DL. Этот простой инструмент для мониторинга серийных результатов от отдельного человека, базируется на предположении, что для того, чтобы изменение было существенным, разница в серийных результатах должна быть больше, чем свойственная вариация как с точки зрения биологической, так и аналитической изменчивости. Наличие надежных данных биологической вариации (BV) является важным для определения спецификаций аналитической эффективности (APS) и необходимым для установления изменения референтного значения (RCV). Европейское исследование биологической вариации (EuBIVAS), которое было разработано в течение последних нескольких лет и все еще продолжается благодаря усилиям Рабочей группы EFLM по BV (WG-BV), предоставило доказательные данные по BV, таким образом позволяя клиническим лабораториям безопасно включать RCV в свои отчеты. Преимущества отчетности о RCV в мониторинге пациентов были продемонстрированы при многих заболеваниях и для многих измеряемых величин, включая опухолевые и костные маркеры, а также в оценке успешности и соответствия терапевтических мероприятий.
Отчет о критических результатах
Одной из главных проблем, связанных с постаналитической деятельностью, является сообщение о критических результатах (CR), которые, по определению, указывают на опасное для жизни состояние со значительным неблагоприятным результатом для пациента, если не принять немедленных спасательных действий. Разработка политики в отношении CRs, которая все еще используется сегодня, стала качественной практикой в процедурах медицинских лабораторий, многие из которых ввели системы для сообщения о CRs.
ІЅО 15189 определяет три требования к отчетности о критических результатах:
- пользователю или другому уполномоченному лицу сообщается как можно скорее на основе имеющейся клинической информации;
- принятые действия задокументированы, включая данные (полученные), время, ответственное лицо, лицо, которое было сообщено, переданные результаты, проверку точности сообщения и любые трудности, возникшие во время сообщения;
- лаборатория должна иметь процедуру эскалации для персонала лаборатории, когда невозможно связаться с ответственным лицом.
Первое требование основывается на доказательствах того, что результат, который демонстрирует риск возникновения опасного для жизни состояния, считается результатом критического риска и должно быть сообщено уполномоченному персоналу как можно быстрее (не более чем через 1 час), тогда как результат указание на потенциальный неблагоприятный результат, который считается результатом значительного риска, может иметь большее время отчетности. В любом случае лаборатория должна иметь процесс отчетности о критических результатах в кратчайшие сроки с помощью надежных и своевременных систем оповещения, чтобы обеспечить своевременное сообщение.
Однако различные используемые терминологии, а также различия в практиках и политиках, описанных в литературе, указывают на необходимость более согласованного и систематического подхода к сообщению о критических результатах. Инициативы по гармонизации должны учитывать следующее:
- надежные пределы значений должны быть выбраны для настоящих «опасных для жизни» аналитов, в соответствии с определением;
- критические значения должны быть сформулированы с учетом характеристик пациентов (то есть возраста, пола и этнического происхождения);
- оповещение должно осуществляться с помощью наиболее эффективных инструментов отчетности и коммуникации;
- должна быть установлена политика, чтобы определить лицо, ответственное за сообщение критических значений, и ответственного за получение этих значений;
- технологические инструменты должны позволять подтверждение критических значений, способствовать обратной связи и записи данных, а также гарантировать, что индикаторы контролируют и контролируют процесс критических значений.
Была четко продемонстрирована ценность сообщения о критических результатах, которое привело к изменению лечения у 98 % пациентов, попавших в хирургические отделения, и у 90,6 % пациентов, попавших в медицинские палаты. Клиницисты провели дополнительную оценку новых осложнений и состояний у 70 и 60,4 % пациентов соответственно в хирургических и медицинских отделениях и приняли дальнейшие меры в стационарном лечении после сообщения о критическом значении. Более тщательный мониторинг клинического состояния больных проводился в 26 % и в 25,5 % случаев в хирургическом и медицинском отделениях соответственно. Клиницисты сообщили, что критические значения были неожиданными находками у 42,3 % пациентов, которые были госпитализированы в хирургические отделения, и 43,0 % пациентов, которые были госпитализированы в медицинские палаты, таким образом подчеркивая ключевую роль, которую играет сообщение о критических результатах в улучшении качества медицинской помощи и безопасности пациентов.
Интерпретационные комментарии
Предоставление советов по интерпретации лабораторных результатов, постаналитическая деятельность, является неотъемлемой частью клинических лабораторных услуг, поскольку правильная клиническая интерпретация лабораторных результатов является желаемым результатом лабораторных услуг.
Клинические, технические и финансовые катализаторы вызвали нынешний спрос на объяснительные комментарии и их желательность. Клинические драйверы включают безопасность пациентов, ценность интерпретационных комментариев, требования к качеству в международных стандартах для аккредитации лабораторий, удовлетворенность врача, новые и сложные лабораторные тесты и образование врача; технические факторы включают отсутствие согласованности лабораторной информации и расширение электронного обмена данными; финансовыми факторами являются конкуренция между клиническими лабораториями и инициативы по сокращению расходов.
Во многих случаях ценность лабораторного результата может быть значительно увеличена с помощью сопроводительного пояснительного комментария:
- неожиданные результаты из-за вмешательства (например, от гетерофильных антител в иммуноанализе);
- определенные находки, обнаруженные в лаборатории (например, макропролактин или макроамилаза);
- расширение первоначального запроса клинициста рефлексивным или рефлективным тестированием (например, идентификация моноклонального пика в электрофорезе сыворотки).
Внедрение новых и сложных тестов в повседневную практику является еще одним главным стимулом для включения пояснительных комментариев в отчет лаборатории. Это особенно верно в некоторых диагностических областях, таких как коагуляция, аутоиммунитет, тестирование на аллергию и молекулярная диагностика, которые являются серьезными проблемами, поскольку требуют передового опыта для правильного толкования лабораторных данных. Кроме того, врачи, которые обращаются с просьбой, все чаще воспринимают объяснительные комментарии, особенно когда они предоставляют клинические советы относительно того, «что делать дальше». Рабочая группа IFCC «Гармонизация оценки качества пояснительных комментариев» опубликовала основополагающий документ, посвященный основным требованиям пояснительных комментариев, включая потребность в образовании, подготовке, соответствующей профессиональной квалификации и опыте для предоставления пояснительных комментариев. Кроме того, была подчеркнута важность специальных схем внешней оценки качества (EQA) для содействия улучшению качества комментариев и, в конечном итоге, результатов для пациентов. Интерпретационные комментарии следует рассматривать как фундаментальную часть стратегии, направленной на совершенствование постаналитического этапа лабораторных исследований, но недавно предоставленные данные также подчеркивают необходимость дальнейших инициатив, направленных на обеспечение качества, гармонизацию и мониторинг интерпретационных комментариев.
Предполагаемые получатели лабораторного отчета
Лабораторные тесты обычно назначаются поставщиком медицинских услуг, отчеты просматриваются врачами, чтобы диагностировать и/или лечить своих пациентов. Оптимальное представление результатов лабораторных исследований в этих случаях в значительной степени зависит от конкретной медицинской ситуации, и большинство рекомендаций, требований и информации, которые должны быть включены в лабораторный отчет, были разработаны с учетом этого типа реципиента. Однако, кроме врачей, результаты лабораторных исследований могут быть представлены и пациентам. Несколько доступных исследований, направленных на определение форматов, которые отвечают потребностям и возможностям пациентов, показывают, что результаты в таких отчетах должны быть обобщены, а их значение должно быть предоставлено четким, понятным и доступным, «немедицинским» языком. По мере того как системы здравоохранения движутся к предоставлению каждому человеку полного доступа к собственным данным, связанным со здоровьем, люди все больше могут получить доступ к результатам своих лабораторных исследований через порталы для пациентов. Потенциальные преимущества этого доступа включают уменьшение нагрузки на пациентов и повышение удовлетворенности пациентов, лечение заболеваний и принятие медицинских решений, но также идут рука об руку с беспокойством по таким вопросам, как результаты, которые вызывают путаницу или беспокойство у пациентов. На самом деле только доступ не может предоставить полной пользы от таких данных и информации, а ошибочная интерпретация лабораторных результатов может вызвать беспокойство пациента, потенциально нанося вред пациенту.
Виттеман и Зикмунд-Фишер определили 10 рекомендаций, чтобы помочь людям превратить данные результатов в значимую информацию и практические знания:
- если это возможно, предоставьте четкое сообщение для каждого результата (сигнализировать, являются ли различия значимыми или нет);
- если это возможно, установите пороговые значения для беспокойства и действия;
- индивидуализируйте систему отсчета, позволяя специальные диапазоны отсчета;
- обеспечьте доступность системы;
- предоставьте инструменты преобразования вместе с результатами;
- проектирование совместно с пользователями;
- дизайн для новых и опытных пользователей;
- сделайте так, чтобы люди могли легко использовать данные по своему желанию;
- сотрудничайте с экспертами из соответствующих отраслей.
Используя лучшие практики для представления лабораторных результатов способом, который помогает людям понять и использовать их, мы можем помочь людям принимать обоснованные решения относительно здоровья и управлять своим здоровьем.
Использование даже самых простых графических линий с числами вместо таблиц для представления результатов теста может уменьшить восприятие пациентом срочность относительно значений, близких к стандартному диапазону, и, следовательно, увеличить чувствительность к вариациям значений теста. Графические визуальные дисплеи могут повысить значимость результатов теста путем четкого определения возможных значений и использования цветных подсказок и оценочных меток: этот тип отчетности данных, который увеличивает возможность пациентов непосредственно получать доступ и просматривать результаты лабораторных тестов, оправдывается концепцией, что благодаря «расширению возможностей пациента» пациенты смогут перевести доступ к тесту, что приводит к лучшей подготовке к клиническим визитам и лучшему самоконтролю болезни, как показано на рисунке ниже.
Графическое представление результатов лабораторных исследований
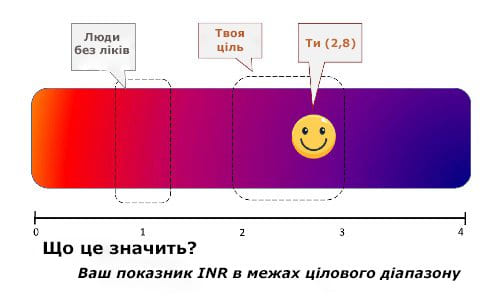
Подытоживая, проблема различных получателей лабораторных отчетов, дополнительная переменная, влияет на сложность согласования постаналитической фазы и, в частности, лабораторного отчета.
Интегративная диагностика и интегрированный отчет
Согласно Всемирной организации здравоохранения (ВОЗ), услуги здравоохранения должны «управляться и предоставляться таким образом, чтобы люди получали непрерывный комплекс услуг укрепления здоровья, профилактики заболеваний, диагностики, лечения, ведения болезней, реабилитации и паллиативной помощи, скоординированные на разных уровнях и местах оказания медицинской помощи в рамках и вне сектора здравоохранения, а также в соответствии с их потребностями на протяжении всей жизни».
«Интегрированная диагностика» (ID) была определена как «конвергенция визуализации, патологии и лабораторных тестов с передовой информационной технологией (IT)». Диагнозы зависят от многих компонентов, которые включают не только визуализацию, но и клиническое наблюдение, патологию, лабораторные и геномные тесты. Центральную роль в медицинской диагностике в настоящее время играют рентгенологические, клинические лаборатории и патологоанатомические отделения, которые выполняют преимущественно диагностические исследования. Однако эти дисциплины не работают как единое целое. Скорее, они являются «островками большого количества данных и чрезвычайного внутридисциплинарного опыта, отделенными друг от друга и от наших клинических коллег информационными, физическими и специальными барьерами». На сегодняшний день существует слишком низкая координация между медицинскими специальностями, ответственными за заказ и проведение этих тестов, а также не уделяется достаточного внимания оптимальному заказу и отчету о тестах. Это изменится в мире интегрированной диагностики, где вместо того, чтобы полагаться на предвзятость отдельных поставщиков в выборе тестов, для определения эффективных диагностических алгоритмов будут использоваться данные из разных источников. Визуализация будет разумно включена в эти интегрированные диагностические алгоритмы, дополняя другие методы диагностики, чтобы максимизировать эффективность и минимизировать отходы. Это, в свою очередь, может обеспечить более быстрый, эффективный и точный процесс принятия клинических решений, что в конечном итоге должно обеспечить лучшие клинические и экономически эффективные результаты. Независимо от клинических и экологических сценариев, несколько линий доказательств сейчас подтверждают роль, которую так называемая «интегрированная диагностика» будет играть в обозримом будущем, позволяя не только более ранние и точные диагнозы, но и экономя значительные человеческие и экономические ресурсы. В своей основополагающей статье по интегративной диагностике Beauchamp и др. отмечают, что «клинические вопросы могут быть решены с помощью диагностической медицины „in vivo“ и „in vitro“, при этом различные дисциплины объединяют свои соответствующие данные и сообщают об интерпретированных результатах другим поставщикам услуг и пациентам в комбинированном отчете». Интегрированные отчеты, объединяющие числовые данные клинических лабораторий с данными патологии и изображений, могут способствовать правильному толкованию и использованию диагностической информации.
Совместная система отчетности о диагностике лаборатории, радиологии и патологии, которая объединяет текст, дозорные изображения и молекулярные диагностические данные в согласованной интерпретации, поможет лучше информировать управленческие решения. Хотя несколько узких мест все еще существуют, интегрированный отчет должен базироваться на стандартизации и, в свою очередь, поощрять ее: междисциплинарное сотрудничество способствует использованию контролируемой терминологии и стандартизированных структур отчетности, что делает возможным оценку во многих когортах пациентов. Рабочие процессы интеграции клинической лаборатории, патологии и радиологии должны обеспечивать эффективную коммуникацию, поток коммуникаций и связывать структурированные результаты диагностики от лабораторий и патологов с результатами радиологов. ID также может привлечь дополнительные человеческие и вычислительные ресурсы для работы с этими, по сути, необработанными данными, таким образом предоставляя информацию, полезную для диагностики и лечения отдельных пациентов, для лечения заболеваний в определенной популяции и для улучшения управления здоровьем.
Искусственный интеллект в постаналитической фазе
Достижения в понимании биологии, патофизиологии болезней и молекулярной медицины в сочетании с технологическим развитием предоставили лабораторной медицине центральную роль, начиная от поддержки благополучия и заканчивая профилактикой заболеваний, ранним выявлением, прогнозом, мониторингом и руководством персонализированной терапии. Пришло время должным образом управлять интерпретацией и использованием огромного количества данных, которые ежедневно генерируют клинические лаборатории, для улучшения ухода за пациентами. Модели алгоритмов принятия решений для отчетности о результатах, системы поддержки клинических решений и искусственный интеллект (ИИ) все больше признаются основными инструментами для достижения этой цели. Компьютеризированные системы поддержки принятия клинических решений (CDSS), которые представляют смену парадигмы в современном здравоохранении, используются для помощи клиницистам в сложных процессах принятия решений и могут быть полезными в лабораторном тестировании и интерпретации. Обеспечение поддержки клинических решений для клиницистов и врачей общей практики приведет к всесторонней интерпретации всех, даже сложных, диагностических процедур в контексте отдельного пациента, таким образом позволяя принять стратифицированное терапевтическое решение.
Интерактивные инструменты машинного обучения были разработаны для улучшения агрегации данных, интерпретации и отчетности о результатах. Эта отрасль, которую в целом называют искусственным интеллектом, но включает в себя различные системы, такие как машинное обучение и искусственные нейронные сети, сейчас привлекает все большее внимание и, несомненно, даст новые идеи и и улучшит ценность лабораторной информации.
Однако, если лабораторные результаты и информация не стандартизированы и гармонизированы, использование машинного обучения, больших данных и, в общем, искусственного интеллекта может быть не только токсичным для многих исследователей в медицине, но также может поставить под угрозу надежность диагнозов и эффективность лечения больного.
Выводы
За последние несколько десятилетий сосредоточение внимания на аналитической фазе позволило лабораторной медицине улучшить качество и гарантию качества. Однако совокупность собранных доказательств показывает, что экстра аналитические фазы уязвимы к ошибкам, в том числе те, которые имеют риск превращения в диагностические ошибки и вреда пациенту. Было приложено немало усилий, чтобы улучшить доаналитическую фазу, тогда как постаналитическая фаза, как представляется, является проблемой, оставленной без внимания. Однако этот последний этап лабораторного тестирования все больше признается фундаментальным шагом в повышении качества и эффективности лабораторной информации: все еще существует потребность замкнуть цикл полного цикла тестирования путем совершенствования как лабораторного отчета, так и его передачи пользователям.
Стоит подчеркнуть важность совершенствования постаналитической фазы, чтобы избежать риска неправильной интерпретации тестов гемостаза, связанных диагностических ошибок и неблагоприятных клинических событий, предлагая стандартизацию/гармонизацию зарегистрированных единиц измерения и референтных диапазонов, а также включение в лабораторные отчеты пояснительных комментариев и своевременной отчетности о критических результатах. Поскольку гармонизация играет фундаментальную роль в улучшении постаналитического этапа, специалисты лаборатории, национальные и международные научные общества и федерации должны усилить свои усилия, чтобы предоставить ценные указания и рекомендации, направленные на улучшение как лабораторного отчета, так и его сообщения пользователю.
Данная информация переведена из статьи Марио Плебани - почетный профессор клинической биохимии и клинической молекулярной биологии Университета Падуи в Италии и профессор кафедры патологии Медицинского отделения Университета Техаса, Галвестон, США.
Plebani M. Гармонизация постаналитической фазы: фокус на лабораторном отчете. Clin Chem Lab Med. 2024 Jan 8. doi: 10.1515/cclm-2023-1402. Epub ahead of print. PMID: 38176022.
Оригинал статьи по ссылке.

Будьте першим, хто залишив відгук на “Согласование постаналитического этапа согласно стандарту ISO 15189:2023”