Хромоэндоскопия в деталях: оборудование, методы, клинические преимущества

Эндоскопия прошла долгий путь — от применения красителей до сложных алгоритмов искусственного интеллекта. Рассмотрим подробнее, как современное оборудование меняет эндовизуализацию.
Хромоэндоскопия — это эндоскопия с использованием красителей для выявления неопластических изменений желудочно-кишечного тракта (ЖКТ) и их классификации на здоровые клетки, предраковые состояния и злокачественные образования [1]. Хромоэндоскопия возникла как ответ на необходимость диагностики скрытых онкологических изменений, которые примерно в 25% случаев могут быть пропущены при проведении классической эндоскопии [2].
Классическая хромоэндоскопия
Традиционная хромоэндоскопия предполагает использование спрей-катетера для нанесения безопасных, нетоксичных красителей на слизистую оболочку желудочно-кишечного тракта (ЖКТ). Реагенты по-разному взаимодействуют со здоровыми, предраковыми и злокачественными клетками, подсвечивая подозрительные участки для максимально точной прицельной биопсии.
В клинической практике используют три типа красителей [1,3]:
- Абсорбционные (витальные) красители. По-разному поглощаются тканями. К ним относятся раствор Люголя, метиленовый синий, уксусная кислота, толуидиновый синий и крезиловый фиолетовый.
- Контрастные красители. Не поглощаются клетками, но оседают в углублениях слизистой оболочки, рельефно выделяя даже минимальные поверхностные изменения (индигокармин).
- Реактивные красители. Меняют свой цвет под воздействием специфических химических процессов внутри раковых клеток (конго красный, феноловый красный).
Виртуальная хромоэндоскопия (NBI/CBI)
Электронная, или виртуальная, хромоэндоскопия полностью исключает необходимость использования спрей-катетеров и химических реагентов. Её действие основано на способности света проникать вглубь тканей с использованием узкоспектральной визуализации (Narrow Band Imaging — NBI, Compound Band Imaging — CBI).
Ключевой принцип технологий NBI/CBI заключается в способности гемоглобина максимально поглощать свет с длиной волны 415 нм [4]. Если при классической хромоэндоскопии врач ориентируется на окрашивание участка, то при виртуальной главным маркером становится рисунок кровеносных сосудов [5]. Коротковолновое излучение контрастирует поверхностный капиллярный рисунок, тогда как длинноволновое проникает глубже и позволяет оценивать подслизистые сосуды [6].
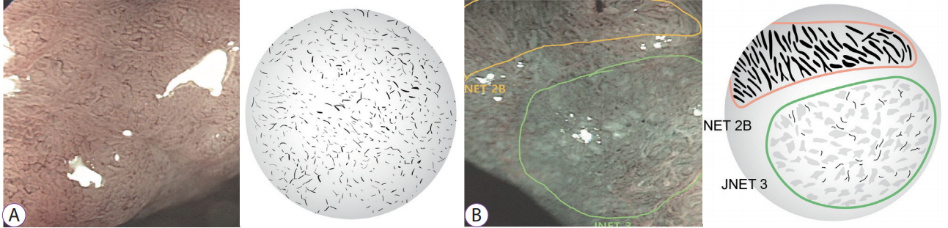
Прогнозирование глубины инвазии выявленного поражения с помощью виртуальной хромоэндоскопии [7].
(A) Поражение имеет капиллярную структуру, характеризующуюся слепым окончанием, неоднородностью и неравномерным сужением, что соответствует структуре Sano IIIA. Это поражение было подтверждено как внутриэпителиальная аденокарцинома.
(B) Слегка углублённый центр поражения демонстрирует разреженные сосудистые участки и аморфную поверхностную структуру. Это поражение было подтверждено как глубоко инвазивная аденокарцинома подслизистого слоя.
Как выбрать систему эндоскопии?
Виртуальная хромоэндоскопия показывает наибольшую эффективность при использовании эндоскопических систем высокого разрешения. Для получения чёткого изображения области визуализации определённого разрешения, например 4K, необходимо, чтобы вся цепочка оборудования поддерживала разрешение 4K. Если монитор, камера или видеопроцессор имеют более низкое разрешение, итоговое качество изображения будет соответствовать наименьшему показателю в системе.
Современные эндоскопические системы классифицируются по количеству светодиодов (LED), генерирующих свет различной длины волны. Чем больше источников света, тем шире возможности виртуальной хромоэндоскопии:
- 5 LED (система AQ 300). Эндоскопическая система с максимальной вариативностью спектров CBI для расширенной диагностики: подсветка кровеносных сосудов подслизистого слоя, структуры слизистой оболочки, контрастирование сосудов на её фоне и визуализация глубоких сосудистых сетей, перекрываемых поверхностными.
- 4 LED (система AQ 200 Elite).
- 3 LED (системи AQ 150 Pro 4K, AQ 120). Оптимальное сочетание разрешения 4K и технологии виртуальной хромоэндоскопии.
- 2 LED (система AQ 100). Базовые модели, излучающие свет 415/540 нм, достаточные для проведения рутинного скрининга.
Искусственный интеллект в эндоскопии
Аппаратные модули искусственного интеллекта функционируют как системы поддержки принятия клинических решений в режиме реального времени, минимизируя влияние человеческого фактора.
Как ИИ-модуль помогает эндоскописту во время процедуры:
- Автоматическая классификация. ИИ в режиме реального времени распознаёт и маркирует предраковые, доброкачественные и злокачественные изменения в зоне осмотра.
- Контроль качества обследования. Система подсказывает оптимальную последовательность осмотра, отмечает уже обследованные участки желудка или кишечника, минимизируя «слепые зоны».
- Контроль скорости. ИИ мгновенно уведомляет врача звуковым или визуальным сигналом, если извлечение эндоскопа происходит слишком быстро.
- Автоматизация рутинных задач. Модуль анализирует время проведения исследования, ведёт запись экрана и автоматически формирует подробный отчёт после завершения процедуры. Это позволяет экономить до 30 % времени врача на подготовке протоколов.
Инвестиции в современное эндоскопическое оборудование с поддержкой виртуальной хромоэндоскопии и искусственного интеллекта напрямую способствуют снижению количества пропущенных карцином и повышению эффективности работы врача.
Источники:
1. Chromoendoscopy. https://www.hopkinsmedicine.org/. URL: https://www.hopkinsmedicine.org/health/treatment-tests-and-therapies/chromoendoscopy.
2. Trivedi P. J., Braden B. Indications, stains and techniques in chromoendoscopy. QJM. 2012. Vol. 106, no. 2. P. 117–131. URL: https://doi.org/10.1093/qjmed/hcs186
3. Chromoendoscopy / L. M. Wong Kee Song et al. Gastrointestinal Endoscopy. 2007. Vol. 66, no. 4. P. 639–649. URL: https://doi.org/10.1016/j.gie.2007.05.029
4. Electronic chromoendoscopy / M. A. Manfredi et al. Gastrointestinal Endoscopy. 2015. Vol. 81, no. 2. P. 249–261. URL: https://doi.org/10.1016/j.gie.2014.06.020
5. Lee H. H., Lee B.-I. Image-Enhanced Endoscopy in Lower Gastrointestinal Diseases: Present and Future. Clinical Endoscopy. 2018. Vol. 51, no. 6. P. 534–540. URL: https://doi.org/10.5946/ce.2018.187
6. Electronic chromo-endoscopy: technical details and a clinical perspective / P. Pal et al. Translational Gastroenterology and Hepatology. 2021. P. 0. URL: https://doi.org/10.21037/tgh-19-373
7. Lee H. H., Lee B.-I. Image-Enhanced Endoscopy in Lower Gastrointestinal Diseases: Present and Future. Clinical Endoscopy. 2018. Vol. 51, no. 6. P. 534–540. URL: https://doi.org/10.5946/ce.2018.187
8. Time Spent on Dedicated Patient Care and Documentation Tasks Before and After the Introduction of a Structured and Standardized Electronic Health Record / E. Joukes et al. Applied Clinical Informatics. 2018. Vol. 09, no. 01. P. 046–053. URL: https://doi.org/10.1055/s-0037-1615747
Будьте першим, хто залишив відгук на “Хромоэндоскопия в деталях: оборудование, методы, клинические преимущества”